|
第九章 电化学基础

(时间90分钟,满分100分)
一、选择题(本题包括16个小题,每小题3分,共48分)
1.(2010・宜昌模拟)某学生设计一水果电池:他把一铁钉和碳棒用导线连接好,然后将
铁钉和碳棒平行插入一新鲜西红柿中,再在导线中接一个灵敏电流计.据此下列叙述正确的是 ( )
A.电流计指针不会发生偏转
B.金属铁会被腐蚀
C.碳棒作负极
D.铁表面有气体逸出
解析:该水果电池中,铁钉为负极,碳棒为正极,电流计指针会发生偏转,碳棒表面产生气泡.
答案:B
2.(2009・江苏高考)以葡萄糖为燃料的微生物燃料电池结构示意图如下图所示.关于该电池的叙述正确的是 ( )
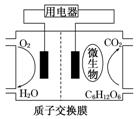
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-===6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体 L
解析:微生物在高温下会因蛋白质变性而死亡,所以该电池不能在高温下工作;该燃料电池的原理为:C6H12O6+6O2===6CO2↑+6H2O,根据总反应方程式可书写出电极反应方程式,负极为C6H12O6+6H2O-24e-===6CO2↑+24H+,正极为6O2+24e-+24H+===12H2O;从电极反应方程式显而易见,H+应从负极移向正极;从总反应方程式可见,每生成1 mol CO2消耗1 mol O2.
答案:B
3.(2009・广州综合测试)以硫酸铜溶液作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼.下列叙述正确的是 ( )
①粗铜与直流电源负极相连
②阴极发生的反应为Cu2++2e-===Cu
③电路中每通过3.01×1023个电子,得到的精铜质量为16 g
④杂质Ag以Ag2SO4的形式沉入电解槽形成阳极泥
A.①③ B.②④
C.③④ D.②③
解析:粗铜作阳极,与电源正极相连;杂质Ag以单质的形式形成阳极泥.
答案:D
4.下列图示中关于铜电极的连接错误的是 ( )

解析:镀件上镀铜时,铜应做阳极,与电源正极相连,镀件做阴极,与电源负极相连.
答案:C
5.如图所示,下列关于实验现象的描述正确的是 ( )
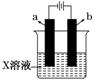
|
|
a电极 |
b电极 |
X溶液 |
实验现象 |
|
A |
石墨 |
石墨 |
CuCl2 |
a电极质量增加,b电极放出无色气体 |
|
B |
Fe |
石墨 |
KNO3 |
a电极质量增加,b电极放出无色气体 |
|
C |
Fe |
Cu |
CuSO4 |
a电极质量增加,b电极质量减少 |
|
D |
石墨 |
石墨 |
HCl |
a电极放出无色气体,b电极放出无色气体 |
解析:这是一个电解装置,其中A、D选项中是惰性电极,且电解液都含有氯离子,所以b电极应该放出淡黄绿色的气体(氯气);B选项中的a电极质量不变;C选项中所组成的电解池相当于电镀池,其中b电极的铜溶解,质量减少,而a电极上析出铜,质量增加.
答案:C
6.观察下列几个装置示意图,有关叙述正确的是 ( )
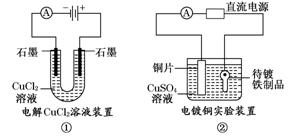
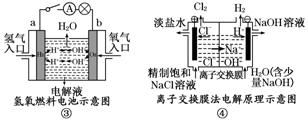
A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源正极相连
C.装置③中外电路电子由a极流向b极
D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
解析:本题考查原电池和电解池的应用.装置①阳极上Cl-放电,发生氧化反应:2Cl--2e-===Cl2↑,A错;装置②待镀铁制品放电,发生还原反应Cu2++2e-===Cu,与电源负极相连,B错;装置④的离子交换膜只允许阳离子自由通过,D错.
答案:C |

