|
�߶����ϣ���ѧ�����Ծ�
һ��ѡ���⣨ÿС��ֻ��һ��ѡ���������, ÿС�� 2 �֣��� 40 �֣�
1������Ƭ��ϡ���ᷴӦ��ȡ����ʱ�����д�ʩ����ʹ�����������ʼӴ����
A. ���� B. ����ϡ���ᣬ����98��Ũ����
C. �μ�����CuSO4��Һ D. ������Ƭ����������
2����Ũ�Ȼ����Һ����������̨Ļ�������Ż���ԭ����
��Ļ�����Ż������  ��Ļ������������ ��Ļ������������
���Ȼ�立ֽ������������������¶� ���Ȼ�立ֽ��������������˿���
A���٢� B���ڢ� C���ۢ� D���ڢ�
3����C��CO2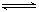 2CO 2CO 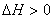 ��Ӧ����Ϊu1��N2��3H2 ��Ӧ����Ϊu1��N2��3H2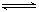 2NH3 2NH3 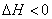 ��Ӧ����Ϊu2������������Ӧ�����¶�����ʱ��u1��u2�ı仯���Ϊ ��Ӧ����Ϊu2������������Ӧ�����¶�����ʱ��u1��u2�ı仯���Ϊ
A. ����С B. ͬʱ���� C. ͬʱ��С D. ��С������
4����һ��6 L���ܱ������У�����3 mol X(g)��2 mol Y(g)����һ�������·������з�Ӧ��4X(g)��3Y(g) 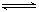 2Q(g)��nR(g) �ﵽƽ����������¶Ȳ��䣬��������ѹǿ��ԭ������5%��X��Ũ�ȼ�С 2Q(g)��nR(g) �ﵽƽ����������¶Ȳ��䣬��������ѹǿ��ԭ������5%��X��Ũ�ȼ�С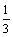 ����÷�Ӧ����ʽ�е�nֵ ����÷�Ӧ����ʽ�е�nֵ
A. 3 B. 4 C. 5 D. 6
5����һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X��g����2Y��g��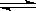 2Z��g���˷�Ӧ�ﵽƽ��ı�־�� 2Z��g���˷�Ӧ�ﵽƽ��ı�־��
A. ������ѹǿ����ʱ��仯
B. �����ڸ����ʵ�Ũ�����
C. ������X��Y��Z��Ũ��֮��Ϊ1�U2�U2
D. ��λʱ������0.1 mol Xͬʱ����0.2 mol Z
6����A g��״̼��Ƹ��������ᷴӦ����Ӧ����ʧ��������ʱ��ı仯��������ͼ��ʵ����ʾ������ͬ�������£���B g ��A��B����ĩ״̼�����ͬŨ�����ᷴӦ������Ӧ�����ߣ�ͼ��������ʾ����ȷ����
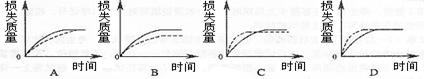
7�������Ȼ�ѧ����ʽ��д��ȷ���ǣ�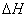 �ľ���ֵ����ȷ�� �ľ���ֵ����ȷ��
A��C2H5OH��l��+3O2��g��==2CO2��g��+3H2O��g������H=-1367.0 kJ/mol��ȼ���ȣ�
B��NaOH��aq��+HCl��aq��==NaCl��aq��+H2O��l������H=+57.3kJ/mol���к��ȣ�[��Դ:ѧ|��|��Z|X|X|K]
C��S��s��+O2��g��==SO2��g������H=-296.8kJ/mol����Ӧ�ȣ�
D�� 2NO2==O2+2NO����H=+116.2kJ/mol����Ӧ�ȣ�
8���ò��缫(����)���������Һʱ�������������ϵ���Ҫ����ֱ���H2��O2����
A. ϡN aOH��Һ B. HCI��Һ C. NaCl��Һ D. ����AgNO3��Һ aOH��Һ B. HCI��Һ C. NaCl��Һ D. ����AgNO3��Һ
9����֪����1 mol H2�����л�ѧ������ʱ��Ҫ����436kJ��������1 mol Cl2�����л�ѧ������ʱ��Ҫ����243kJ����������Hԭ�Ӻ�Clԭ���γ�1 mol HCl����ʱ�ͷ�431kJ������������������ȷ����
��A��������������Ӧ�����Ȼ���������Ȼ�ѧ����ʽ��H2(g)��Cl2(g)��2HCl(g)
��B��������������Ӧ����2 mol�Ȼ������壬��Ӧ����H��+183kJ/mol
��C��������������Ӧ����1 mol�Ȼ������壬��Ӧ����H����183kJ/mol
��D��������������Ӧ����2mol�Ȼ������壬��Ӧ����H����183kJ/mol
10����֪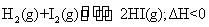 ����ͬ�ݻ��Ķ����ܱ��������ң����м��� ����ͬ�ݻ��Ķ����ܱ��������ң����м���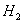 �� ��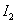 ��1mol �����м���HI2mol����ͬ�¶��·ֱ�ﵽƽ�⡣��ʹ����HI��ƽ��Ũ�ȴ�������HI��ƽ��Ũ�ȣ�Ӧ��ȡ�Ĵ�ʩ�� ��1mol �����м���HI2mol����ͬ�¶��·ֱ�ﵽƽ�⡣��ʹ����HI��ƽ��Ũ�ȴ�������HI��ƽ��Ũ�ȣ�Ӧ��ȡ�Ĵ�ʩ��
A���ס��������ͬ�¶� B ���м���1mol He���Ҳ���
C�������¶ȣ��Ҳ��� D ������1mol 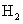 ��������1mol ��������1mol 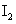 |

