|
2011中考化学难点攻略:――金属的化学性质
【课标要求】
●知道常见的金属与氧气的反应;
●能用金属活动性顺序表对有关的置换反应进行简单的判断,并能解释日常生活中的一些现象。
【核心内容】
1.镁、铝、铁、铜与氧气的反应,铝制品表面致密氧化膜的形成。
 ①通过实验探究了解金属活动性顺序。 ①通过实验探究了解金属活动性顺序。
2.金属活动性顺序 ②应用:判断金属与酸、金属与盐溶液是否发生置换反应。
③根据反应事实及现象,判断某种未知金属的活动性。
 ①能正确判断某反应是否是置换反应。 ①能正确判断某反应是否是置换反应。
②利用置换反应的知识解释日常生活中的有关化学问题和现象。
【要点精讲】
1.金属与氧气的反应
大多数金属都能与氧气反应,但反应的难易和剧烈程度不同,Mg、Al等在常温下就能与氧气反应;Fe、Cu等在常温时几乎不与氧气反应,金在高温是也不与氧气反应。其有关化学反应方程式分别为:
2Mg+O2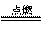 2MgO;4Al+3O2 2MgO;4Al+3O2 2Al2O3;3Fe+2O2 2Al2O3;3Fe+2O2 Fe3O4;2Cu+O2 Fe3O4;2Cu+O2 2CuO。 2CuO。
2.金属的活动性顺序
 (1)记忆法: (1)记忆法:
在记忆金属活动性顺序时,可将其分成如下三组帮助记忆:①钾钙钠镁铝;②锌铁锡铅氢;
③铜汞银铂金。
(2)三条规律: 金属活动性顺序表主要反映以下三条规律:①在金属活动性顺序表里,金属的位置越靠前,它的活动性就越强;②排在氢前面的金属能置换出盐酸 |

