|
高考化学试题解题策略
策略 4 速率与平衡方面试题的解题方法与技巧
金点子:
在化学反应中物质的变化必经过三态,即起始态、变化态和最终态。对于化学反应速率、化学平衡及其它化学反应方面的计算,如能根据反应方程式,对应地列出三态的变化,哪么便可使分析、解题变得一目了然。此方面的试题的题型及方法与技巧主要有:
1.化学平衡状态的判断
化学反应是否达到平衡状态,关键是要看正反应速率和逆反应速率是否相等及反应混合物中各组分百分含量是否还随时间发生变化。
2.化学反应速率的计算与分析
要充分利用速率之比等于化学方程式中的计量数之比。
3.化学平衡移动的分析
影响因素主要有:浓度、压强、温度,其移动可通过勒沙特列原理进行分析。化学平衡移动的实质是浓度、温度、压强等客观因素对正、逆反应速率变化产生不同的影响,使V正≠V逆,原平衡状态发生移动。
4.等效平衡的分析
主要有等温等容和等温等压两种情况。
5.速率与平衡的图象分析
主要要抓住三点,即起点、拐点和终点。
经典题:
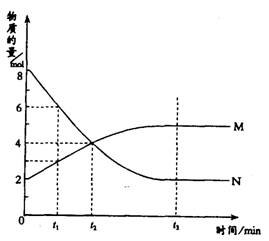
例题1:(2001年全国高考)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是 ( )
A.反应的化学方程式为:2M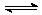 N N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
方法:图象分析法。
捷径:从图中得到N为反应物,M为生成物。从0→t2min,M增加2mol,N消耗4mol,且到达t3min,M、N的浓度保持不变,即反应为可逆反应,反应式为 。t2时反应物和生成物物质的量相等,此时不是正、逆反应速率相等。当t3时正逆反应的速率相等。t1时n(N)=6mol,n(M)=3mol,由于在同一容器中,所以c(N)=2c(M)。因此此题正确答案为D。 。t2时反应物和生成物物质的量相等,此时不是正、逆反应速率相等。当t3时正逆反应的速率相等。t1时n(N)=6mol,n(M)=3mol,由于在同一容器中,所以c(N)=2c(M)。因此此题正确答案为D。
总结:选项B最容易被误认为正确说法。造成错判的原因有三:①没有看清纵坐标的物理量;②概念错误,认为物质的量相等时,化学反应速率就相等;③没有读懂图。
例题2 :(1998年全国高考)体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应: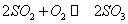 ,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率 ( ) ,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率 ( )
A.等于p% B.大于p% C.小于p% D.无法判断
方法:平衡中的等效转化分析法。
捷径:设乙容器压强保持1.01×105Pa,因甲容器中体积保持不变,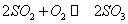 的正反应是个气体体积缩小的反应,达到平衡时,混合气体的总压强小于1.01×105Pa。又减小压强,平衡向逆反应方向移动,则甲容器中SO2转化率低,乙容器中(定压)SO2的转化率高。以此得答案为B。 的正反应是个气体体积缩小的反应,达到平衡时,混合气体的总压强小于1.01×105Pa。又减小压强,平衡向逆反应方向移动,则甲容器中SO2转化率低,乙容器中(定压)SO2的转化率高。以此得答案为B。
总结:将两平衡态先相联系,再依据平衡移动原理相互转化,便能快速方便获得结果。
例题3 :(2002年全国高考)在一定温度下,向a L密闭容器中加入1 mol X气体和2mol Y气体,发生如下反应: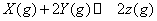 。 。
此反应达到平衡的标志是 ( )
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为l : 2 : 2
D.单位时间消耗0.1 mol X的同时生成0.2 mol Z
方法:从平衡状态下正逆反应速率相等分析。
捷径:此反应为一气体分子数减小的反应,故容器内压强不随时间变化,说明巳达平衡。各物质的浓度不随时间变化而变化,说明正逆反应速率相等,巳达平衡状态。浓度为一固定比值不能说明巳达平衡。D项中的所述均为正反应,未提到逆反应,故不能判断。以此得答案为AB。
总结:平衡状态的判断,是高考中的重点内容,也是平衡中的重点。此类试题只要抓住平衡状态下速率相等,各成分的百分含量保持不变,即可求解。 |

