|
应用・习题精练
1.下列说法中不正确的是( )
A.1 mol某气体的体积为22.4 L,该气体所处的状态不一定是标准状况
B.非标准状况下,1 mol任何气体的体积可能是22.4 L
C.某气体含有NA个原子,该物质在标准状况下的体积一定是22.4 L
D.任何状况下,1 mol CO2和1 mol H2O所含的分子数和原子数都相等
解析:本题主要考查气体摩尔体积概念的内涵和本质。尤其要注意标准状况下22.4 L・mol-1的使用。因为在非标准状况下,1 mol气体的体积也可能为22.4 L,所以A、B正确;当气体为单原子分子的稀有气体时符合C选项,而双原子或多原子分子不符合,C错;因为比较粒子数实质是比较它们的物质的量,所以D正确。
答案:C
2.(2010北京东城检测)NA代表阿伏加德罗常数,下列说法正确的是( )
A.常温常压下,22.4 L H2所含氢原子数目为2NA
B.1.8 g NH+4所含电子数目为NA
C.58.5 g NaCl晶体中所含的氯化钠分子数目为NA
D.1 L 1 mol・L-1 Na2CO3溶液中所含的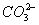 数目为NA 数目为NA
解析:A.常温常压下,不能应用22.4 L・mol-1进行计算。C.NaCl是离子晶体,无分子存在,存在的是离子。D.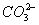 水解,使其数目减少。 水解,使其数目减少。
答案:B
3.下列条件下,两种气体的分子数一定不相等的是( )
A.相同质量、不同密度的N2和C2H4
B.相同体积、相同密度的CO和C2H4
C.相同温度、相同压强、相同体积的O2和N2
D.相同压强、相同体积、相同质量的O2和N2
解析:A.N2和C2H4的摩尔质量相同,相同质量的N2和C2H4,物质的量相同,分子数也相同。
B.相同体积、相同密度的CO和C2H4,具有相同的质量,同时也具有相同的分子数。
C.同温同压下同体积的任何气体具有相同的分子数。
D.同质量的O2和N2,摩尔质量不同,物质的量不同,从而分子数不相等,故D错误。
答案:D
4.(2010江苏南通检测)NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol HNO3见光分解,转移电子数4NA
B.28 g晶体硅中含有Si―Si键的数目为2NA
C.100 mL 0.5 mol・L-1的(NH4)2SO4溶液中,含有0.1NA个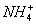
D.Cu与浓硝酸产生的22.4 L(标准状况)气体中含原子数为3NA
解析:由4HNO3====2H2O+4NO2↑+O2↑知,1 mol HNO3完全分解可转移1 mol电子,但由于见光只是部分分解,故A错。由于NH+4在水溶液中水解,故NH+4数小于0.1 mol,C错。Cu与浓HNO3反应,主要产物是NO2,但也有少量NO,故22.4 L气体中所含原子数会少于3 mol,D错。B正确。
答案:B
|

