|
习题精练
1.下列叙述正确的是( )
A.离子化合物中可能含有共价键
B.共价化合物中可能含有离子键
C.金属离子都一定满足最外电子层2或8电子结构
D.共价化合物中各原子都一定满足最外层8电子结构
解析:离子化合物如NaOH中氢氧之间为共价键;具有离子键的化合物一定是离子化合物,不可能是共价化合物,A正确,B错。Fe2+最外层有14个电子,故C不正确。共价化合物HCl中H原子不满足8电子结构,D不正确。
答案:A
2.(2010北京西城检测)下列说法正确的是( )
A.离子化合物中一定不含共价键
B.共价化合物中一定不含离子键
C.两种元素组成的化合物中一定不含非极性键
D.由于水分子之间存在氢键,所以水分子比较稳定
解析:本题考查物质结构与化学键的知识,离子化合物中可含有共价键,A错误;两种元素组成的化合物中可含有非极性键,如:Na2O2,C错误;分子稳定与分子间力无关,D错误;B正确。
答案:B
3.下列物质中,既含有离子键,又含有非极性共价键的是( )
A.NaOH B.Na2O2 C.CaCl2 D.H2O
解析:NaOH中含离子键,OH-中含极性共价键。Na2O2含离子键,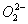 中含非极性键,CaCl2中只含离子键,H2O中只含极性键。 中含非极性键,CaCl2中只含离子键,H2O中只含极性键。
答案:B
4.(2010广东中山统一检测)已知白磷(P4)是一个内空的正四面体结构,四个磷原子处于四个顶点(如图52所示),白磷被氧化可生成六氧化四磷(P4O6),六氧化四磷的分子中只有单键,且每个原子的最外层都满足8个电子的结构,则该分子中含有共价键的数目是( )
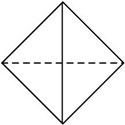
图5-2
A.10 B.12 C.24 D.28
解析:根据白磷的结构可知,P4O6可看作白磷分子中每个磷磷键中插入一个氧原子而得,又已知该分子中只含有单键,因此P4O6分子中含有的共价键数目为6×2=12。
答案:B
5.根据下列实验事实,确认某晶体一定是离子晶体的是( )
A.晶体熔点达2500 ℃ B.晶体不导电,溶于水能导电
C.晶体不导电,熔融能导电 D.温度越高,溶解度增大
解析:离子晶体、原子晶体、金属晶体的熔点一般都比较高,故A不正确。离子晶体、原子晶体、分子晶体不导电,但离子晶体和某些分子晶体溶于水后能导电,B不正确。一般情况下,温度升高,物质〔除气体、Ca(OH)2外〕的溶解度增大,D不正确。
答案:C
|

