|
习题精练
1.有关氨的说法不正确的是( )
A.NH3是4核10电子极性分子,三角锥形,具有还原性
B.NH3极易溶于水,可做喷泉实验,氨气易液化,液氨可用作制冷剂
C.氨气是非电解质,氨水是电解质
D.蘸有浓盐酸的玻璃棒遇氨气可产生白烟
解析:NH3分子中氮元素-3价是最低价态,因此NH3具有还原性,A正确;根据相似相溶原理知极性分子NH3易溶于极性溶剂H2O,氨的蒸发热很大,可作制冷剂,B正确;电解质、非电解质都指化合物,而氨水是混合物,故C不正确;浓盐酸与NH3作用产生白色晶体NH4Cl,故D正确。
答案:C
2.(2010山东潍坊质检)在下列几种物质中:①NaHCO3、②Al(OH)3、③(NH4)2CO3、④SiO2、⑤金属铝、⑥Al2O3,其中与HCl溶液和NaOH溶液都能发生反应的是( )
A.只有②④⑥ B.只有①⑤⑥
C.只有①②③⑤⑥ D.全部都可以
解析:二氧化硅只能与氢氧化钠反应而不能与盐酸反应,因此只能选C。
答案:C
3.用加热方法可分离的一组物质是( )
A.氯化铵和消石灰 B.碳铵和过氧化钠
C.碘和食盐 D.硝酸铵和硫酸钠
解析:氯化铵与消石灰发生反应产生NH3、H2O和CaCl2,显然无法分离。碳铵加热分解同时与过氧化钠发生反应。硝酸铵受热分解产物更复杂,故答案为C。
答案:C
4.在标准状况下,在三个干燥的烧瓶内分别装入有干燥纯净的NH3、含一半空气的氯化氢气体、NO2和O2的混合气体〔V(NO2)∶V(O2)=4∶17〕。然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2∶1∶2 B.5∶5∶4
C.1∶1∶1 D.无法确定
解析:NH3、HCl溶于水后,溶液的体积即为被溶解了的气体体积,c=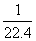 mol・L-1。由4NO2+O2+2H2O====4HNO3可知,当O2过量时,每消耗4 mol NO2、1 mol O2,则生成4 mol HNO3,c(HNO3)= mol・L-1。由4NO2+O2+2H2O====4HNO3可知,当O2过量时,每消耗4 mol NO2、1 mol O2,则生成4 mol HNO3,c(HNO3)=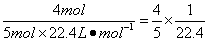 mol・L-1。故答案为B。 mol・L-1。故答案为B。
答案:B
5.下列铵盐①NH4F ②NH4Cl ③NH4Br ④NH4I,其热稳定性由强到弱的顺序为( )
A.④>③>②>① B.①>②>③>④
C.①>④>③>② D.无法确定
解析:铵盐受热分解的过程就是铵根离子(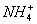 )把质子转移给酸根的过程,对于题目所给四种同类型的铵盐,酸根离子半径越小,结合H+能力越强,则盐就越不稳定,答案为A。 )把质子转移给酸根的过程,对于题目所给四种同类型的铵盐,酸根离子半径越小,结合H+能力越强,则盐就越不稳定,答案为A。
答案:A
6.A是一种白色晶体,它与浓NaOH溶液共热,放出无色气体B。用圆底烧瓶收集干燥的B,按图8-2所示装置仪器,挤压滴管的胶头时,可以得到蓝色喷泉;A与浓H2SO4反 |

