|
习题精练
1.下列对硝酸的认识不正确的是( )
A.浓硝酸和稀硝酸都具有氧化性 B.铜和稀硝酸的反应属于置换反应
C.金属与硝酸反应一定不产生氢气 D.常温下可用铝或铁制品盛装浓硝酸
解析:硝酸是强氧化性酸,且浓硝酸的氧化性强于稀硝酸,A正确。由铜与浓、稀硝酸反应的方程式看,均不属于置换反应;因为硝酸是强氧化性酸,金属与硝酸反应均不生成H2,而生成水。D之所以正确,是由于浓硝酸可使铝和铁的表面生成一层致密的氧化膜,阻止反应进一步进行,但是在加热情况下,铝和铁可以与浓硝酸反应。
答案:B
2.现有下列物质:①氯水 ②氨水 ③浓硝酸④氢氧化钠 ⑤溴,其中必须保存在棕色瓶里的是( )
A.全部 B.①③和⑤ C.①和③ D.①②和④
解析:氯水见光发生反应2HClO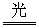 2HCl+O2↑而变质,浓硝酸见光分解:4HNO3 2HCl+O2↑而变质,浓硝酸见光分解:4HNO3 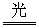 4NO2↑+O2↑+2H2O,为防止它们分解变质,必须储存在棕色瓶里。 4NO2↑+O2↑+2H2O,为防止它们分解变质,必须储存在棕色瓶里。
答案:C
3.(2010山东潍坊质检)将足量的铜屑加入到浓度均为2 mol・L-1的HNO3和H2SO4的混合溶液100 mL中,充分反应后,转移电子的物质的量为( )
A.0.6 mol B.0.8 mol C.0.45 mol D.0.4 mol
解析:反应的离子方程式为:3Cu+8H++2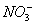 ====3Cu2++2NO↑+4H2O ====3Cu2++2NO↑+4H2O
HNO3与H2SO4的混合液中共有H+0.6 mol,共有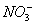 0.2 mol。 0.2 mol。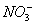 过量,参加反应的 过量,参加反应的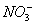 为0.15 mol,转移的电子为0.45 mol。 为0.15 mol,转移的电子为0.45 mol。
答案:C
4.(2010天津河西检测)已知单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为:aFe+b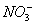 +cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)。若a=12,且铁和硝酸恰好完全反应,则b的取值范围是( ) +cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)。若a=12,且铁和硝酸恰好完全反应,则b的取值范围是( )
A.6 B.3048 C.8 D.6
解析:若a=12,当金属铁全部转化为Fe2+时,失去电子的数目为24e-,当金属铁全部转化为Fe3+时,失去电子的数目为36e-,故金属铁失电子的数目范围为(24,36)。若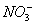  NO,则有24<3b<36,即8若 NO,则有24<3b<36,即8若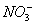  N2O,则有24<4b<36,即6。要注意取并集,因此b的取值范围是6。 N2O,则有24<4b<36,即6。要注意取并集,因此b的取值范围是6。
答案:A
5.在含有1 mol HNO3和2 mol H2SO4的混合稀溶液中,加入1.5 mol Cu,加热,充分反应后产生的气体体积在标准状况下约为( )
A.5.6 L B.11.2 L C.22.4 L D.44.8 L
解析:因Cu与稀硝酸反应:3Cu+8HNO3====3Cu(NO3)2+2NO↑+4H2O
由化学方程式可知Cu过量,这时H2SO4中的H+与Cu(NO3)2的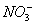 组合成HNO3再与 组合成HNO3再与 |

