|
第二节 水的电离和溶液的酸碱性
一、选择题(包括8小题。1~6小题只有一个选项符合题意,7~8小题有两个选项符合题意。)
1.(2008年上海卷)常温下,某溶液中由水电离的c(H+)=1×10-13 mol・-1L,该溶液可能是( )
①二氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液
④氢氧化钠水溶液
A.①④
B.①②
C.②③
D.③④
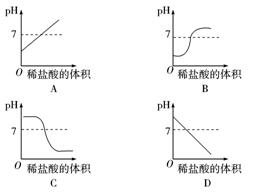
2.向盛有10 mL NaOH溶液的烧杯中逐滴滴加稀盐酸,下列图象能够体现溶液的pH变化情况的是( )
3.在由水电离产生的H+的浓度为1×10-13 mol・-1L的溶液中,一定能大量共存的离子组是( )
①K+、Cl-、NO3-、S2- ②K+、Fe2+、I-、SO42- ③Na+、Cl-、NO3-、SO42- ④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-
A.①③
B.③⑤
C.③④
D.②⑤
4.常温下,0.1 mol・-1L某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-10,下列叙述正确的是( )
A.溶液中水电离出的c(H+)=10-10 mol・-1L
B.溶液中c(H+)+c(A-)=0.1 mol・-1L
C.与0.05 mol・-1L NaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
D.上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
5.25 ℃时,pH=3的盐酸a L分别与下列三种溶液充分混合后,溶液均呈中性:①c(NH3・H2O)=10-3 mol・-1L的氨水b L,②c(OH-)=10-3 mol・-1L的氨水c L,③c(OH-)=10-3 mol・-1L的Ba(OH)2溶液d L。试判断a、b、c、d的数量大小关系为( )
A.a=b>c>d
B.b>a=d>c
C.b>a>d>c
D.c>a=d>b
6.(2009年济南模拟)取pH均为2的盐酸和醋酸各100 mL,分别加水稀释两倍后,再分别加入6.5 g锌粉,相同条件下充分反应,下列说法中,不正确的是( )
A.加水稀释后两溶液的pH不再相等
B.起始时醋酸与锌反应的速率大
C.醋酸与锌反应放出的氢气多
D.两者放出的氢气一样多
7.(2010年枣庄检测)MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中正确的是 ( )
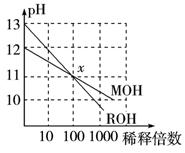
A.在x点时,ROH完全电离
B.在x点时[M+]=[R+]
C.MOH是一种强碱
D.稀释前,[ROH]=10[MOH] |

