|
2011高考化学解题方法系列专题4・平均摩尔电子质量
一、 摩尔电子质量
⒈ 摩尔电子质量:每转移一摩尔电子所需反应物的质量。]
⑴金属单质的摩尔电子质量:数值上等于某金属的相对原子质量除以该金属在反应中表现的化合价。如:Fe在与盐酸的反应中其摩尔电子质量为 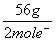 = = 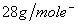 ,在与氯气的反应中其摩尔电子质量为 ,在与氯气的反应中其摩尔电子质量为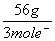 = =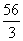 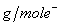
⑵非金属单质的摩尔电子质量:数值上等于某非金属单质的相对分子质量除以1mol该非金属 单质在反应中获得的电子数。 单质在反应中获得的电子数。
⑶化合物的摩尔电子质量:数值上等于某化合物的相对分子质量除以1mol该化合物在反应中得(失)的电子数。
⑷在某一具体反应中不参与氧化还原反应的物质其摩尔电子质量视为无穷大。如:将铁铜合金投入到盐酸中,铜不与盐酸反应,其摩尔电子质量为无穷大。
⒉ 平均摩尔电子质量:混合物的总质量除以反应中混合物得失电子的总数。
二、摩尔电子质量法的应用
⒈ 判断混合物的组成
例⒈ 某合金15g,在足量氯气中充分燃烧,反应后固体质量增加了35.5g,则合金的组成可能是( )[来源:学,科,网Z,X,X,K]
A. Fe、Al B. Mg、Al C. Cu、Mg D. Fe、Zn
解析:在此反应中Fe、Mg、Al、Cu、Zn的摩尔电子质量分别为18.67、12、9、32、32.5。合金的平均摩尔电子质量为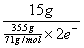 =15 =15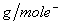 ,由中间数值法得A、C两项正确。 ,由中间数值法得A、C两项正确。
例⒉ 由Na、Mg、Al、Fe四种金属单质中的两种组成的合金共12g,跟足量盐酸反应,产生5.6LH2(标况),由此可判断混合物中必定含有( )
A.Na B.Mg C.Al D.Fe
解析:Na、Mg、Al、Fe的摩尔电子质分别为23、12、9、28,混合物的平均摩尔电子质量是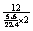 =24,只有Fe的摩尔电子质量大于24,故必有Fe。 =24,只有Fe的摩尔电子质量大于24,故必有Fe。
例3:锰的氧化物MnO2、Mn2O3、Mn3O4、Mn2O7在加热时均能和浓盐酸发生反应生成MnCl2 和Cl2,现有11.45g锰的某种氧化物与足量的盐酸反应,产生的氯气在标准状况下的体积为1.12升,则参加反应的氧化物是( )
A.MnO2 B.Mn2O3 C.Mn3O4 D.Mn2O7 解析:由题意可知,该锰的氧化物的摩尔电子质量为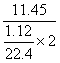 =114.5。考查各选项,MnO2的摩尔电子质量为 =114.5。考查各选项,MnO2的摩尔电子质量为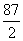 =43.5,Mn2O3的摩尔电子质量为 =43.5,Mn2O3的摩尔电子质量为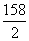 =79,Mn3O4的摩尔电子质量为 =79,Mn3O4的摩尔电子质量为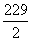 =114.5, =114.5, Mn Mn 2O7的摩尔电子质量为 2O7的摩尔电子质量为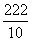 =22.2,所以应选C。 =22.2,所以应选C。 |

